近日,动物医学院王林教授团队在《journal of advanced research》发表了题为“cadmium targeting transcription factor eb to inhibit autophagy-lysosome function contributes to acute kidney injury”的研究论文。动物医学院已毕业硕士生董鹏飞为该论文第一作者,王林教授为该论文的通讯作者。
镉(cd)是生态环境中一种常见的重金属污染物,主要通过食物链的富集作用对人类和动物健康造成严重危害。cd也是一种蓄积性毒物,对机体的损伤呈多系统性和多器官性。肾脏是镉最重要的蓄积部位和靶器官,职业性镉暴露可引起急性肾损伤。目前aki的发病机制复杂,其中自噬-溶酶体功能障碍在aki发病过程中发挥重要作用。转录因子eb(tfeb)已被证明是溶酶体生物发生和自噬相关基因转录的关键调控因子。然而,tfeb在cd诱导aki中的潜在机制尚不清楚。因此,阐明tfeb在cd所诱导自噬-溶酶体功能障碍中的作用对于缓解aki具有重要意义。如图1结果所示,cd诱导的肾小管上皮细胞损伤和自噬-溶酶体功能障碍可通过tfeb的药理激活剂或基因过表达得到缓解,而沉默tfeb基因则加剧其损伤。本研究结果强调了cd通过抑制tfeb功能导致自噬-溶酶体功能障碍而促进aki的病理学进程。
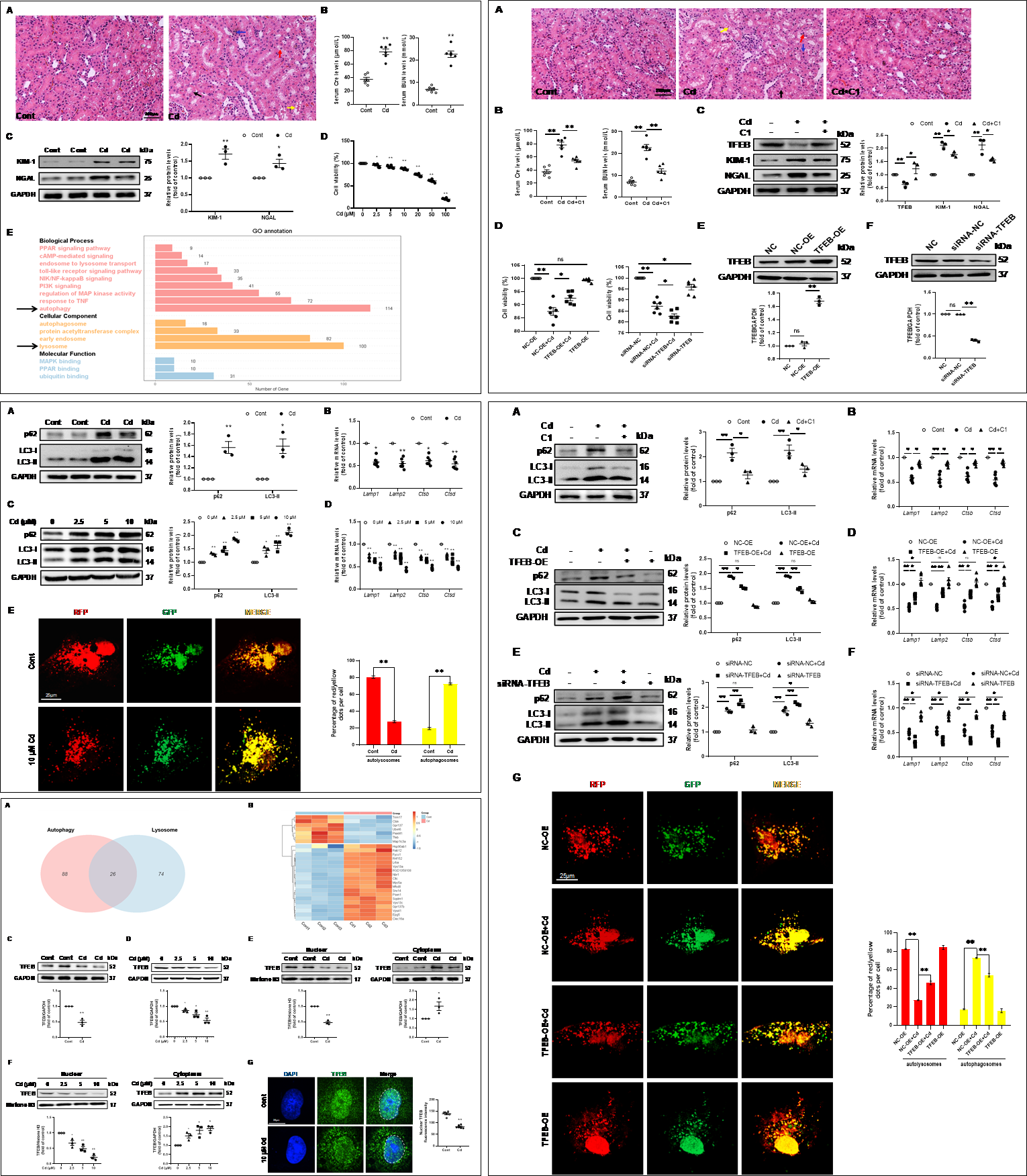
图1 tfeb依赖性自噬-溶酶体功能障碍促进cd诱导的急性肾损伤
从机制上讲,cd激活雷帕霉素复合体1(mtorc1)增强tfeb磷酸化,从而抑制tfeb核易位;cd也激活染色体区域维持1(crm1)促进tfeb核输出。同时,cd激活组蛋白乙酰转移酶gcn5增强核tfeb乙酰化,导致tfeb转录活性降低。研究结果表明,cd对tfeb活性的抑制依赖于mtorc1介导的tefb磷酸化、crm1介导的tfeb核输出和gcn5介导的tfeb乙酰化的联合作用,但tfeb磷酸化、核输出和乙酰化分别通过抑制tfeb活性促进自噬-溶酶体功能障碍,共同参与了cd诱导的aki。这些研究结果解析了cd诱导肾损伤的潜在分子机制(图2),阐明了tfeb是cd诱导aki的一个潜在治疗靶点。
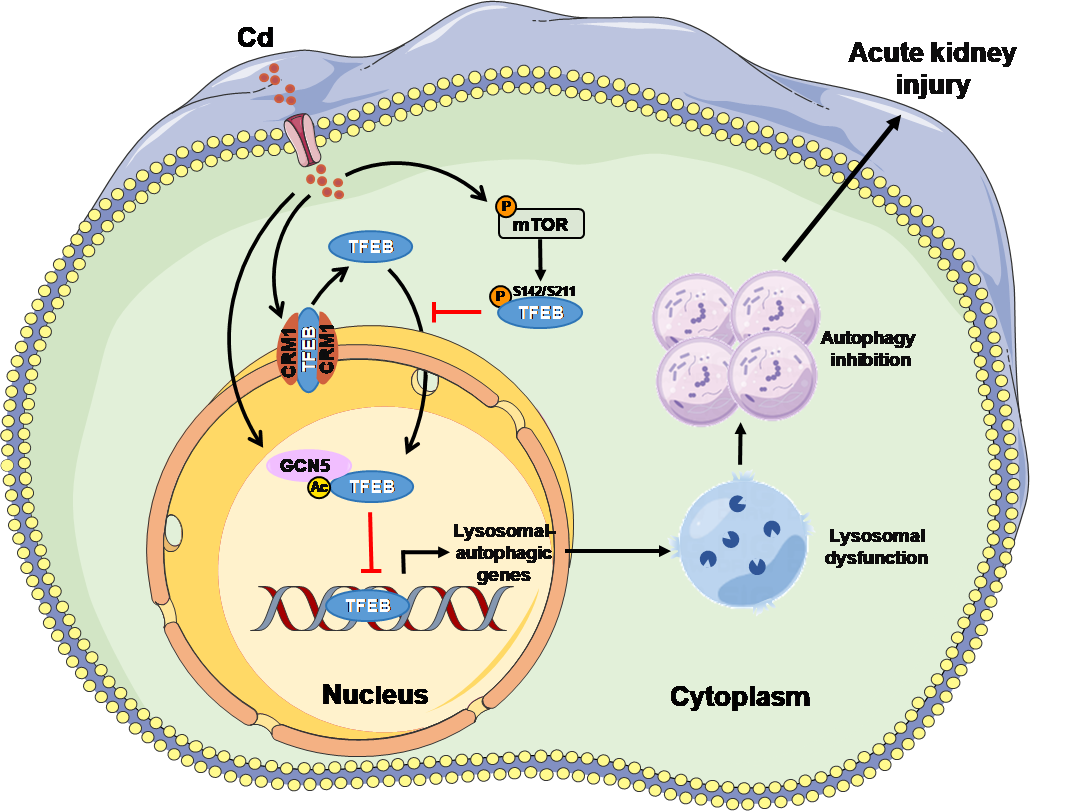
图2 cd靶向tfeb抑制自噬-溶酶体功能导致aki的示意图
本研究得到了国家自然科学基金面上项目和山东省高等学校青创科技计划创新团队项目资助。
全文链接:https://doi: 10.1016/j.jare.2024.07.013.
编 辑:万 千
审 核:贾 波




